UvA-scheikundigen ontwikkelen nanodeeltjes voor kankertherapie
UvA-hoogleraar Hong Zhang en -postdoc Yansong Feng combineren met hun onderzoek naar nanodeeltjes twee soorten therapieën om dieper gelegen tumoren te bestralen. Het eerste preklinische onderzoek in muizen heeft al aangetoond dat de nieuwe therapie werkt. Ze publiceerden de resultaten begin dit jaar in wetenschapstijdschrift Journal of Materials Chemistry C.
Twee veelvoorkomende behandelingen voor kanker kennen ook twee grote nadelen. Uitwendige radiotherapie, het behandelen van kanker door röntgenstraling, heeft als grote voordeel dat de röntgen dwars door alle weefsels heen gaat, maar als nadeel dat de therapie niet gericht is en ook gezonde cellen aantast. Fotodynamische therapie, het behandelen van kanker door bestraling met licht, is vooral geschikt voor huidkanker omdat het licht niet verder dan twee centimeters door de huid kan dringen en diepgelegen tumoren niet kan bereiken. Hoogleraar Hong Zhang en postdoc Yansong Feng van de onderzoeksgroep Molecular Photonics combineerden de voordelen in een nieuwe therapie via nanodeeltjes.

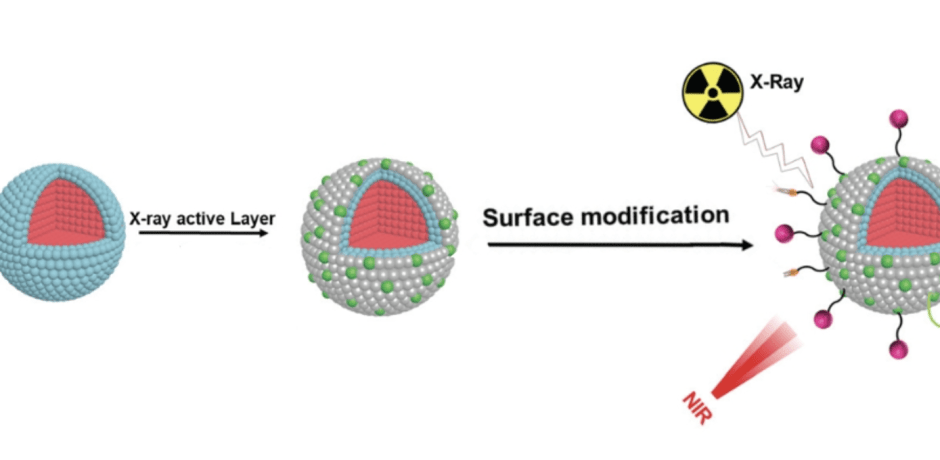
De onderzoekers ontworpen nanodeeltjes die onder invloed van röntgenstraling zelf zichtbaar licht kunnen uitstralen voor fotodynamische therapie. Daarnaast kunnen de deeltjes bij bestraling met nabij infraroodlicht (NIRNabij infraroodlicht bevindt zich met golflengtes tussen 750 en 1000 nanometer net naast het zichtbare lichtspectrum (380 tot 800 nanometer) met een kleine overlap.) ook nog eens dieprood uitstralen, waardoor de plaats van de tumor oplicht en artsen een lagere dosis röntgenstraling gerichter kunnen toedienen. Hong Zhang: ‘De tumor wordt zo tegelijkertijd behandeld met radio- en fotodynamische therapie. Dat verhoogt de efficiëntie en veroorzaakt minder bijeffecten.’
De nanodeeltjes worden geïnjecteerd in de bloedbaan en zijn zo klein dat ze door alle weefsels heen kunnen bewegen. Met behulp van een tumorspecifiek antilichaam op de buitenste schil spoort het deeltje de tumor op. De buitenste laag is ook in staat om röntgenstraling om te zetten in zichtbaar licht. De kern, die met een bufferlaag wordt gescheiden van de buitenlaag, kan NIR omzetten in rood licht voor de lokalisatie. Zhang: ‘NIR heeft een golflengte van 1.000 nanometer, die gaat naar een kortere golflengte van rood licht met een hogere energie. De energie gaat dus omhoog, in plaats van naar beneden, daarom noemen we het upconversie.’ Die twee processen verstoren elkaar niet.
‘We zien nu een toepassing voor kanker,’ vertelt Zhang, ‘maar de potentiele toepassingen voor de nanodeeltjes gaan veel verder.’ De therapie kan ook gebruikt worden als geneesmiddel voor bacterie- of virusinfecties, simpelweg door een ander antilichaam te gebruiken. ‘Dat werkt in principe hetzelfde.’
Geen wishful thinking
Nanodeeltjes voor kankertherapie is geen wishful thinking. Na onderzoek in levende cellen laat ook preklinisch onderzoek in muizen al zien dat het werkt. De onderzoekers vroegen al een Europees en internationaal patent aan op de techniek. Om de volgende stap te kunnen maken moeten meer data verkregen worden met diermodellen. ‘Dat ligt buiten onze expertise’, legt Zhang uit. ‘Daar hebben we de hulp van ziekenhuizen bij nodig.’
Daarom werken de onderzoekers samen met netwerkplatform Innovation Exchange Amsterdam om investeerders en medische partners te vinden. De onderzoekers hebben al reacties ontvangen. Zhang: ‘Daar zijn we blij mee. Via hen kunnen we communiceren met de betrokken partijen. Dat helpt.’